Die zugelassene Altersgruppe für die Anwendung von Clonidin transdermal ist 18 Jahre und älter.Es ist ausdrücklich nicht für Personen unter 18 Jahren zugelassen.Das Clonidin Transdermales Pflaster wurde 1984 von der FDA zur Behandlung von leichtem bis mittelschwerem Bluthochdruck, entweder allein oder in Kombination mit einem Diuretikum, zugelassen und wirkt als zentral wirkender Alpha-Agonist blutdrucksenkend.
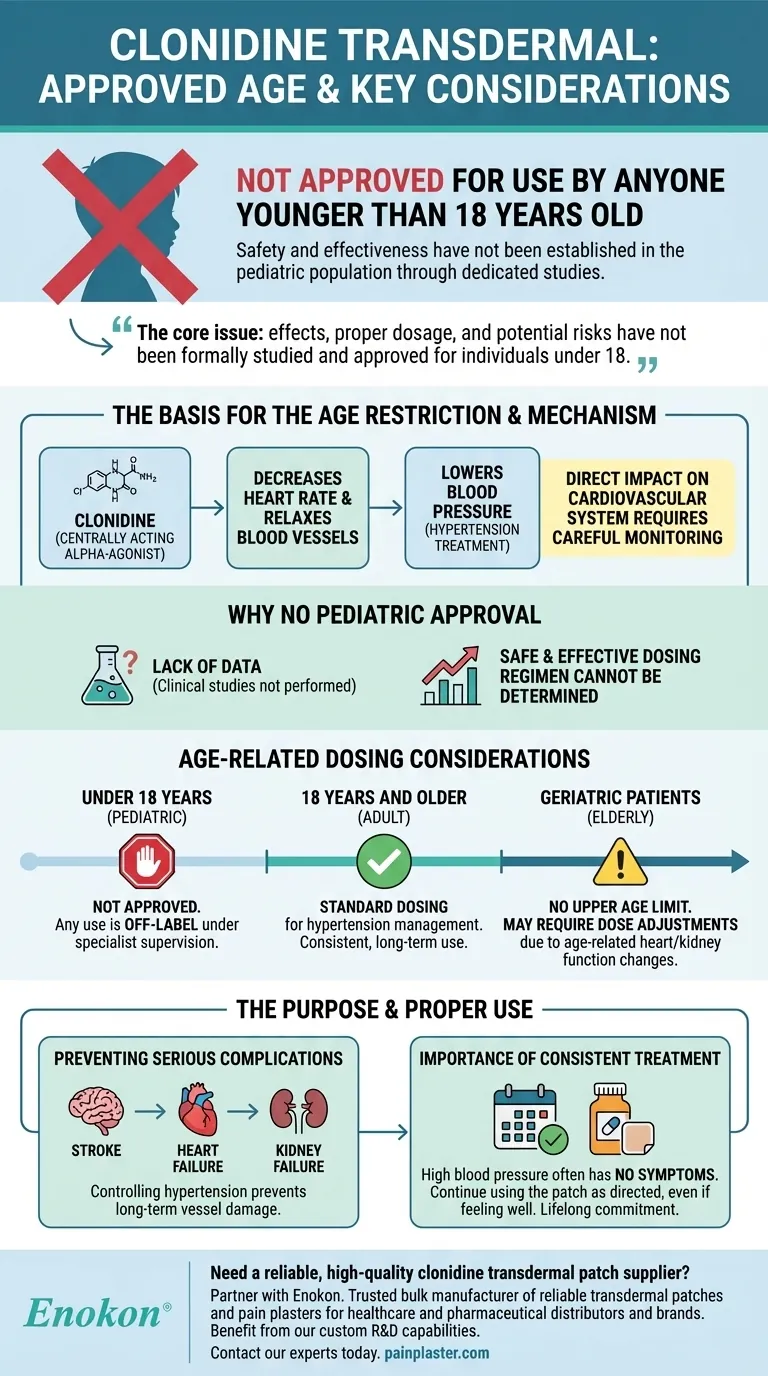
Die wichtigsten Punkte werden erklärt:
-
FDA-zugelassene Altersbeschränkung
- Clonidin transdermal ist nicht für Patienten unter 18 Jahren zugelassen .Diese Einschränkung wird in mehreren Verweisen wiederholt, was ihre Bedeutung für die klinische Anwendung unterstreicht.
- Das Pflaster ist speziell für Erwachsene (ab 18 Jahren) indiziert, wahrscheinlich aufgrund unzureichender Daten zur Sicherheit/Wirksamkeit in pädiatrischen Bevölkerungsgruppen oder möglicher Risiken, die nur für jüngere Patienten gelten.
-
Primäre medizinische Anwendung
- Zugelassen zur Behandlung von leichter bis mäßiger Hypertonie (Bluthochdruck), entweder als Monotherapie oder in Kombination mit einem Diuretikum.
- Sein Wirkmechanismus besteht darin, dass es als zentral wirkender Alpha-Agonist der die Aktivität des sympathischen Nervensystems reduziert, um den Blutdruck zu senken.
-
Regulatorischer Hintergrund
- Die FDA genehmigte die transdermale Formulierung im 1984 und spiegelt damit seine langjährige Rolle bei der Behandlung von Bluthochdruck wider.
- Die Altersbeschränkung ist seit der Zulassung unverändert geblieben, was darauf hindeutet, dass es keine weiteren Belege für die Verwendung bei Kindern gibt.
-
Klinische Erwägungen für Einkäufer
- Gesundheitsdienstleister, die das Pflaster kaufen, müssen das Alter der Patienten überprüfen, um eine Off-Label-Anwendung bei Kindern zu vermeiden.
- Die Einschränkung bedeutet, dass für pädiatrische Patienten möglicherweise alternative blutdrucksenkende Therapien erforderlich sind.
Diese Klarheit gewährleistet die Einhaltung der Verschreibungsrichtlinien und die Sicherheit der Patienten.Für die erwachsene Bevölkerung bietet das Pflaster eine nicht-orale Option zur Blutdruckkontrolle - ein Detail, das für die Entscheidungsträger in der Rezeptur wichtig ist.
Zusammenfassende Tabelle:
| Hauptaspekt | Einzelheiten |
|---|---|
| Zugelassener Altersbereich | 18 Jahre und älter (nicht für die pädiatrische Verwendung) |
| Primäre Anwendung | Behandlung von leichtem bis mäßigem Bluthochdruck |
| Mechanismus der Wirkung | Zentral wirkender Alpha-Agonist zur Senkung des Blutdrucks |
| FDA-Zulassung Jahr | 1984 |
| Klinische Erwägungen | Überprüfen Sie das Alter des Patienten; für Patienten unter 18 Jahren sind alternative Therapien erforderlich |
Benötigen Sie zuverlässige transdermale Lösungen für die Behandlung von Bluthochdruck bei Erwachsenen?
Enokon ist auf die Massenproduktion von hochwertigen transdermalen Pflastern, einschließlich Clonidin-Formulierungen, für Gesundheitsdienstleister und Pharmamarken spezialisiert.Unser Know-how gewährleistet die Einhaltung der FDA-Richtlinien und die nahtlose Integration in Ihre Produktlinie.
Kontaktieren Sie uns noch heute um über kundenspezifische F&E, Großbestellungen oder regulatorische Unterstützung zu sprechen - lassen Sie uns gemeinsam die Patientenversorgung verbessern.
Visuelle Anleitung
Ähnliche Produkte
- Ferninfrarot-Wärmepflaster zur Schmerzlinderung Transdermale Pflaster
- Silikonpflaster für Narbenblätter Transdermales Medikamentenpflaster
- Icy Hot Menthol Medizin Schmerzlinderung Patch
- Menthol Gel Schmerzlinderungspflaster
- Beifuß-Wermut-Pflaster zur Schmerzlinderung bei Nackenschmerzen
Andere fragen auch
- Welche Rolle spielen transdermale Pflaster bei der Verbesserung von Hautläsionen? Entdecken Sie, wie Stabilisierung Druckgeschwüre verhindert
- Welche Faktoren beeinflussen die Wirksamkeit von transdermalen Pflastern?Wichtige Überlegungen für eine optimale Wirkstoffabgabe
- Wie trägt hochreines Ferninfrarot-Keramikpulver zur Wirksamkeit von Ferninfrarot-Physiotherapie-Pflastern bei?
- Wie verbessern transdermale Pflaster die Therapietreue?Verbesserte Therapietreue mit Leichtigkeit
- Welche Rolle spielt ein Exsikkator bei der Feuchtigkeitsgehaltsanalyse von transdermalen Pflastern? Gewährleistung von Stabilität und Sicherheit











