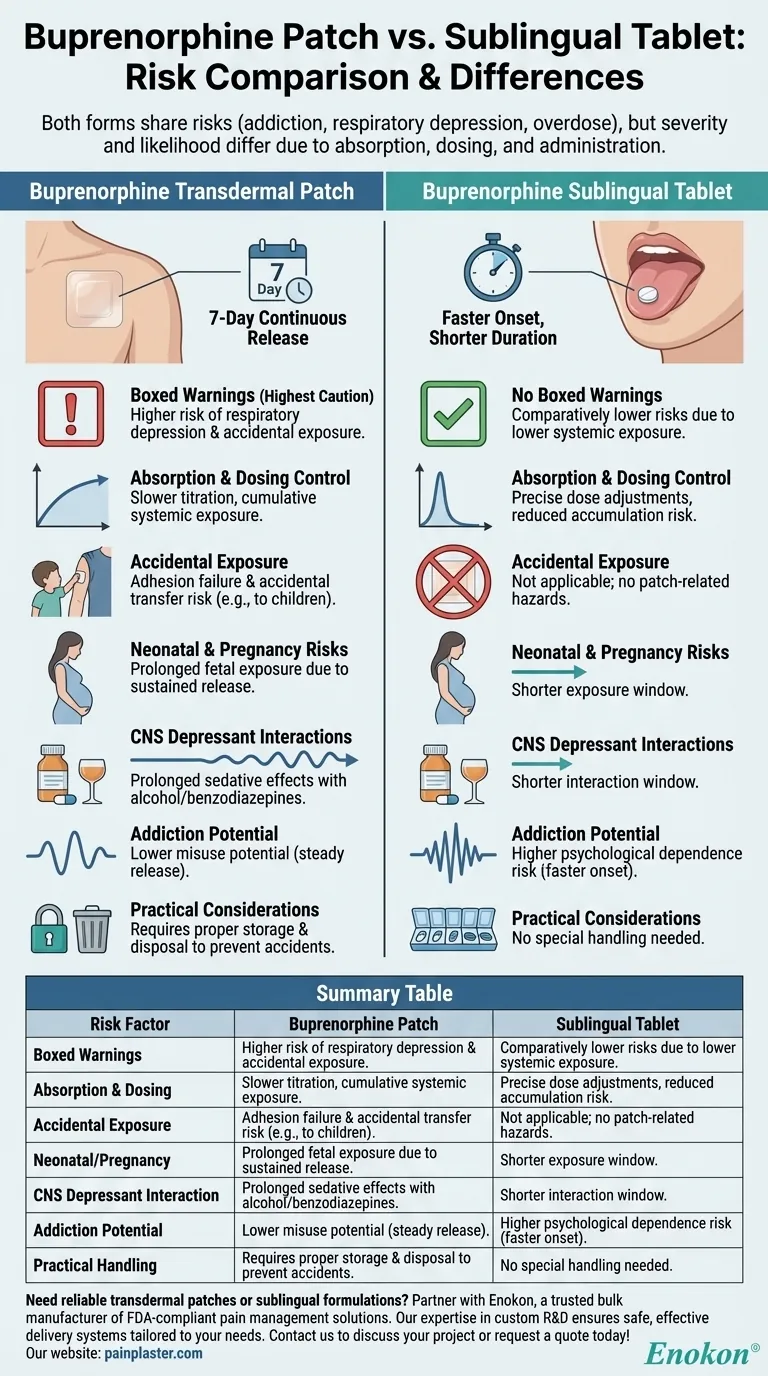
Buprenorphin ist, unabhängig davon, ob es als transdermales Pflaster oder als sublinguale Tablette verabreicht wird, mit Risiken wie Abhängigkeit, Atemdepression, versehentlicher Überdosierung, neonatalem Opioid-Entzugssyndrom und Wechselwirkungen mit ZNS-Depressiva verbunden.Schweregrad und Wahrscheinlichkeit dieser Risiken unterscheiden sich jedoch zwischen den beiden Formulierungen.Das Buprenorphin-Transdermalpflaster birgt höhere Risiken, die einen Warnhinweis rechtfertigen, während die Sublingualtablette zwar nicht ohne Risiken ist, diese aber aufgrund der Unterschiede bei der Absorption, der Dosierungskontrolle und der Verabreichungsmethode geringer ausfallen.

Die wichtigsten Punkte werden erklärt:
-
Warnhinweise und Schwere der Risiken
- Das transdermale Pflaster hat Warnhinweise im Kasten (die schärfste Warnstufe der FDA) aufgrund des höheren Risikoprofils, insbesondere im Hinblick auf Atemdepression und versehentliche Exposition (z. B. durch unsachgemäße Entsorgung des Pflasters oder Kontakt mit Kindern).
- Bei der Sublingualtablette fehlen die Warnhinweise, da die Risiken vergleichsweise geringer, aber dennoch vorhanden sind.Dies spiegelt die Unterschiede in der systemischen Exposition und der Dosierungsgenauigkeit wider.
-
Absorption und Dosierungskontrolle
- Pflaster:Verabreichung einer kontinuierlichen Dosis über 7 Tage, was zu einer kumulativen systemischen Exposition und langsamere Titrationsanpassungen.Dies erhöht das Risiko einer anhaltenden Atemdepression oder einer Überdosierung bei Missbrauch.
- Tablette:Sublinguale Absorption mit schnellerem Wirkungseintritt und kürzerer Dauer, was eine präzisere Dosisanpassung ermöglicht und das Risiko einer Kumulation verringert.
-
Unbeabsichtigte Exposition
- Das Pflaster birgt einzigartige Risiken wie Versagen der Adhäsion (was zu unbeabsichtigter Dosierung führt) oder versehentliche Übertragung (z. B. an ein Kind durch Hautkontakt).Diese Szenarien sind für Tabletten nicht relevant.
-
Risiken für Neugeborene und Schwangere
- Bei beiden Formen besteht das Risiko neonatales Opioid-Entzugssyndrom Die verlängerte Freisetzung des Pflasters kann jedoch die Exposition des Fötus verschlimmern, wenn es während der Schwangerschaft verwendet wird.
-
Wechselwirkungen mit ZNS-Dämpfungsmitteln
- Das Risiko besteht für beide Formen, aber die verzögerte Freisetzung des Pflasters kann die sedierende Wirkung verlängern, wenn es mit Alkohol oder Benzodiazepinen kombiniert wird.
-
Suchtpotenzial
- Zwar können beide Formulierungen süchtig machen, aber der schnellere Wirkungseintritt der Tablette könnte für manche Patienten ein höheres psychisches Abhängigkeitsrisiko darstellen, während die gleichmäßige Freisetzung des Pflasters das Missbrauchspotenzial verringern könnte.
-
Praktische Erwägungen
- Das Pflaster muss ordnungsgemäß gelagert und entsorgt werden, um eine versehentliche Exposition zu verhindern, was zusätzliche logistische Risiken mit sich bringt, die bei Tabletten nicht auftreten.
Zusammenfassend lässt sich sagen, dass beide Formulierungen zwar die gleichen Kernrisiken aufweisen, das Pflaster jedoch aufgrund seiner längeren Wirkungsdauer und des Potenzials für Gefahren im Zusammenhang mit der Nichteinhaltung der Einnahme strengere Warnhinweise erfordert.Die kürzer wirkende Tablette bietet mehr Kontrolle, erfordert aber eine wachsame Dosierungsfrequenz.Kliniker müssen diese Unterschiede gegen patientenspezifische Faktoren wie Compliance und Missbrauchsrisiko abwägen.
Zusammenfassende Tabelle:
| Risikofaktor | Buprenorphin-Pflaster | Sublinguale Tablette |
|---|---|---|
| Warnhinweise im Kasten | Ja (höheres Risiko einer Atemdepression, versehentliche Exposition) | Nein (geringeres systemisches Risiko) |
| Absorption und Dosierung | Kontinuierliche Freisetzung über 7 Tage; langsamere Titration, höheres Risiko einer kumulativen Exposition | Schnellerer Wirkungseintritt, kürzere Dauer; einfachere Dosisanpassung |
| Unbeabsichtigte Exposition | Hoch (Versagen der Verklebung, Übertragung auf andere) | Gering (keine pflasterbedingten Gefahren) |
| Neonatal/Schwangerschaft | Verlängertes Risiko für den Fötus | Kürzeres Expositionsfenster |
| Wechselwirkung mit ZNS-Dämpfungsmitteln | Verlängerte sedierende Wirkung | Kürzeres Interaktionsfenster |
| Suchtpotenzial | Geringeres Missbrauchspotenzial (gleichmäßige Freisetzung) | Höheres psychisches Abhängigkeitsrisiko (schnellerer Beginn) |
| Praktische Handhabung | Erfordert sichere Lagerung/Entsorgung | Keine besondere Handhabung erforderlich |
Sie benötigen zuverlässige transdermale Pflaster oder sublinguale Formulierungen? Partner mit Enokon ist ein zuverlässiger Hersteller von FDA-konformen Lösungen für die Schmerzbehandlung.Unser Know-how in der kundenspezifischen Forschung und Entwicklung gewährleistet sichere, wirksame Verabreichungssysteme, die auf Ihre Bedürfnisse zugeschnitten sind. Kontaktieren Sie uns um Ihr Projekt zu besprechen oder noch heute ein Angebot anzufordern!
Visuelle Anleitung
Ähnliche Produkte
- Menthol Gel Schmerzlinderungspflaster
- Lidocain-Hydrogel-Pflaster zur Schmerzlinderung
- Icy Hot Menthol Medizin Schmerzlinderung Patch
- Far Infrared Pain Patch Relief Schmerzmittel für Rücken
- Asthma-Husten- und Schmerzlinderungspflaster für Erwachsene und Kinder
Andere fragen auch
- Wann sollten Sie die Verwendung von Schmerzmitteln wie Cremes und Pflastern in Betracht ziehen?Optimieren Sie Komfort und Sicherheit
- Können schwangere Frauen Schmerzpflaster verwenden?Sicherheit und Alternativen erklärt
- Welche verschiedenen Arten von Schmerzpflastern gibt es?Finden Sie die richtige Lösung für Ihre Schmerzen
- Was sind einige gängige Anwendungen von Schmerzpflastern?Gezielte Linderung für die Schmerzbehandlung
- Sind rezeptfreie Schmerztabletten und -pflaster erhältlich?OTC-Optionen erklärt