Das Buprenorphin-Transdermales Pflaster ist mit vier kritischen Warnhinweisen der FDA versehen, die auf die schwerwiegendsten Risiken hinweisen: Sucht-/Missbrauchspotenzial, Gefahr einer versehentlichen Exposition, lebensbedrohliche Atemdepression und neonatales Opioid-Entzugssyndrom.Diese Warnungen betonen die Notwendigkeit strenger Verschreibungsprotokolle, die Aufklärung der Patienten über die ordnungsgemäße Entsorgung des Pflasters und die Überwachung auf Atembeschwerden - insbesondere bei der ersten Anwendung oder bei Dosisänderungen.Die opioiden Eigenschaften des Medikaments erfordern auch Vorsicht bei der Einnahme von ZNS-Depressiva und Alkohol, während schwangere Patientinnen riskieren, ihr Neugeborenes Entzugserscheinungen auszusetzen.Häufige Nebenwirkungen wie Hautreizungen stehen im Gegensatz zu seltenen, aber schweren Reaktionen wie Herzrhythmusstörungen oder Anaphylaxie.
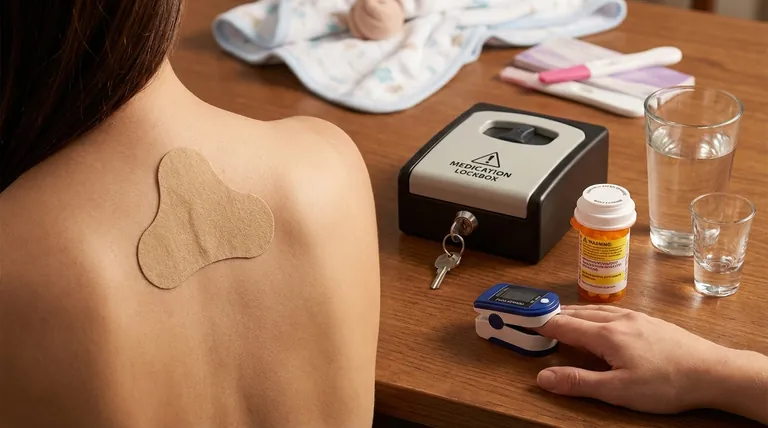
Die wichtigsten Punkte werden erklärt:
-
Sucht-, Missbrauchs- und Misshandlungspotenzial
- Als partieller Opioid-Agonist birgt das Pflaster das Risiko der Abhängigkeit und der illegalen Abzweigung.
- Ein längerer Gebrauch erhöht die Toleranz und erfordert ein vorsichtiges Absetzen, um einen Entzug zu vermeiden.
- Verordner sollten vor Beginn der Einnahme die Vorgeschichte des Patienten in Bezug auf Substanzkonsumstörungen prüfen.
-
Versehentliche Exposition
- Unbenutzte Pflaster müssen gefaltet (Klebeseiten zusammen) und ausgespült werden, um den Zugang von Kindern/Haustieren zu verhindern.
- Eine sekundäre Exposition durch Hautkontakt (z. B. durch Umarmen eines Pflasterbenutzers) kann bei gefährdeten Personen eine Atemdepression auslösen.
-
Lebensbedrohliche Atemwegsdepression
- Das höchste Risiko besteht innerhalb von 72 Stunden nach der Anwendung oder Dosiseskalation.
- Die gleichzeitige Einnahme von Benzodiazepinen, Alkohol oder anderen ZNS-Depressiva erhöht die Gefahr exponentiell.
- Patienten mit COPD oder Schlafapnoe müssen verstärkt überwacht werden.
-
Neonatales Opioid-Entzugssyndrom (NOWS)
- Eine längere fetale Exposition während der Schwangerschaft kann bei Neugeborenen zu Krampfanfällen, schlechter Nahrungsaufnahme oder Tod führen.
- Erfordert eine spezialisierte neonatale Intensivpflege, um das Opioid nach der Geburt schrittweise abzusetzen.
-
Zusätzliche kritische Erwägungen
- Hautreaktionen:An den Applikationsstellen kann es zu schweren Reizungen oder Verbrennungen kommen, die einen Wechsel und das Meiden von Wärmequellen erfordern.
- Wechselwirkungen mit Arzneimitteln:CYP3A4-Inhibitoren (z. B. Erythromycin) können den Buprenorphinspiegel erhöhen und damit das Toxizitätsrisiko steigern.
- Beseitigungsprotokoll:Die FDA empfiehlt, die Spülung der Müllentsorgung vorzuziehen, um eine versehentliche Exposition zu vermeiden - ein wichtiger Beratungspunkt für Apotheker.
Diese Warnungen unterstreichen, warum dieses Medikament eine sorgfältige Auswahl der Patienten, eine informierte Zustimmung und eine laufende Nutzen-Risiko-Bewertung erfordert.Wie könnten diese Zwänge die Verschreibungsentscheidungen in der ambulanten Schmerzbehandlung beeinflussen?
Zusammenfassende Tabelle:
| Black Box Warnung | Hauptrisiken und Vorsichtsmaßnahmen |
|---|---|
| Sucht-/Missbrauchspotenzial | Risiko der Abhängigkeit, illegale Abzweigung; erfordert eine Beurteilung der Patientenanamnese und ein Absetzen. |
| Versehentliche Exposition | Nicht verwendete Pflaster falten und abspülen; sekundärer Hautkontakt kann Atemdepression verursachen. |
| Atemdepression | Höchstes Risiko in den ersten 72 Stunden; ZNS-depressive Substanzen (z. B. Alkohol, Benzodiazepine) vermeiden. |
| Neonatales Entzugssyndrom | Kann bei Neugeborenen zu Krampfanfällen oder zum Tod führen; erfordert eine Behandlung auf der Intensivstation für Neugeborene zum Absetzen. |
| Zusätzliche Risiken | Schwere Hautreizungen, Arzneimittelwechselwirkungen (CYP3A4-Inhibitoren), strenge Entsorgungsprotokolle. |
Benötigen Sie zuverlässige Lösungen für die transdermale Schmerzbehandlung? Partner mit Enokon ist ein zuverlässiger Hersteller von FDA-konformen transdermalen Pflastern und Schmerzpflastern in großen Mengen.Unser Fachwissen in der kundenspezifischen Forschung und Entwicklung gewährleistet sichere, wirksame Formulierungen, die auf Ihre Bedürfnisse zugeschnitten sind - ideal für Vertriebsunternehmen im Gesundheitswesen und pharmazeutische Marken. Kontaktieren Sie uns noch heute um Ihre Projektanforderungen zu besprechen oder Muster anzufordern!
Visuelle Anleitung

Ähnliche Produkte
- Ferninfrarot-Wärmepflaster zur Schmerzlinderung Transdermale Pflaster
- Icy Hot Menthol Medizin Schmerzlinderung Patch
- Menthol Gel Schmerzlinderungspflaster
- Silikonpflaster für Narbenblätter Transdermales Medikamentenpflaster
- Beifuß-Wermut-Pflaster zur Schmerzlinderung bei Nackenschmerzen
Andere fragen auch
- Welche Rolle spielen transdermale Pflaster bei der Verbesserung von Hautläsionen? Entdecken Sie, wie Stabilisierung Druckgeschwüre verhindert
- Wie verbessern transdermale Pflaster die Therapietreue?Verbesserte Therapietreue mit Leichtigkeit
- Wie trägt hochreines Ferninfrarot-Keramikpulver zur Wirksamkeit von Ferninfrarot-Physiotherapie-Pflastern bei?
- Welche Faktoren beeinflussen die Wirksamkeit von transdermalen Pflastern?Wichtige Überlegungen für eine optimale Wirkstoffabgabe
- Welche Rolle spielt ein Exsikkator bei der Feuchtigkeitsgehaltsanalyse von transdermalen Pflastern? Gewährleistung von Stabilität und Sicherheit