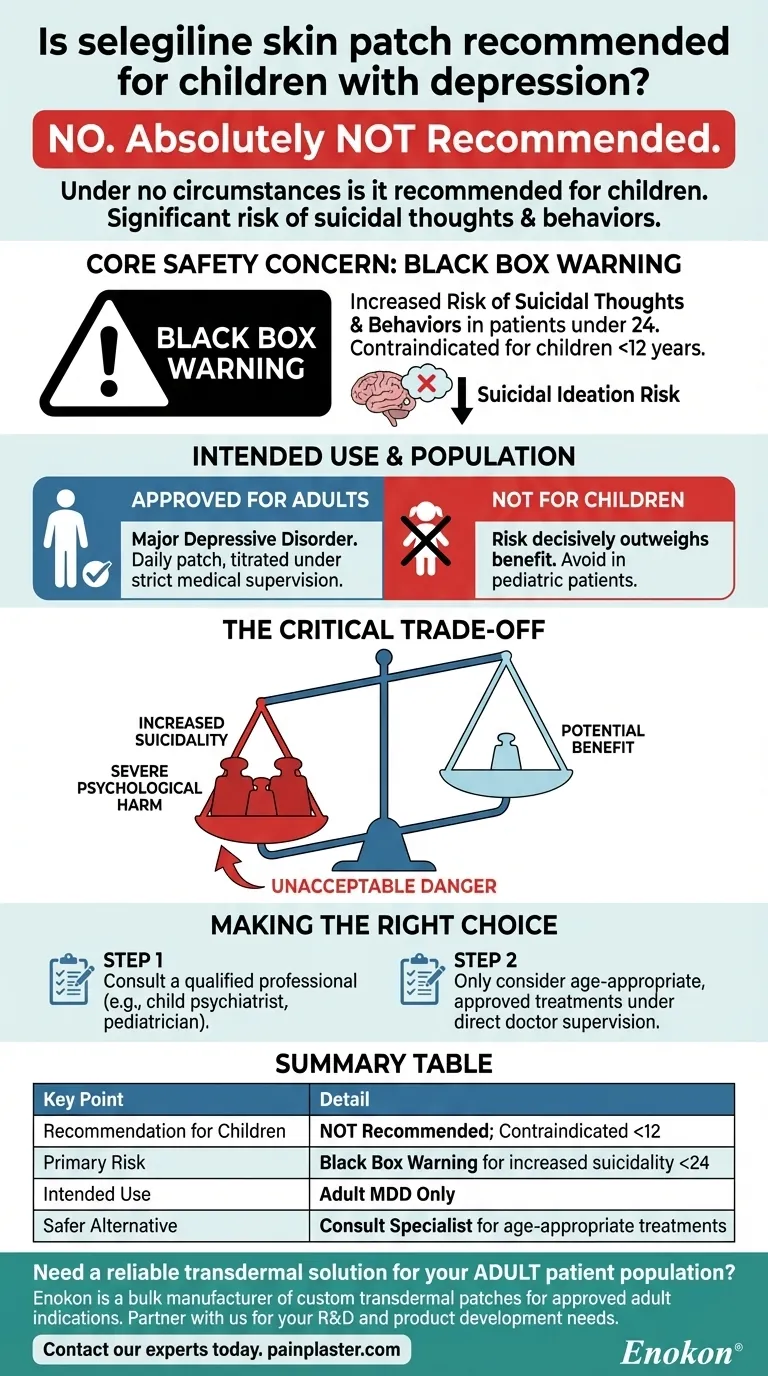
Das Selegilin-Hautpflaster wird für die Behandlung von Depressionen bei Kindern nicht empfohlen, da erhebliche Sicherheitsbedenken bestehen, insbesondere wegen des Risikos von Selbstmordgedanken oder -versuchen in der pädiatrischen Bevölkerungsgruppe.Klinische Nachweise und Verschreibungsrichtlinien raten durchweg von der Anwendung bei Kindern unter 12 Jahren ab, wobei weitergehende Vorsichtsmaßnahmen auch für Jugendliche und junge Erwachsene gelten.Auch das Verabreichungsprotokoll des Medikaments (6-12 mg/24 Stunden über die intakte Haut) stellt für die pädiatrische Anwendung eine praktische Herausforderung dar.

Die wichtigsten Punkte werden erklärt:
-
Kontraindikation für die Anwendung bei Kindern
- Selegilin transdermale Pflaster werden in mehreren maßgeblichen Quellen ausdrücklich für Kinder unter 12 Jahren kontraindiziert.Diese Einschränkung basiert eher auf dokumentierten Sicherheitsprofilen als auf Dosierungsbeschränkungen.
-
Erhöhtes Suizidrisiko
- Klinische Studien zeigen, dass bei Kindern, Jugendlichen und jungen Erwachsenen, die Antidepressiva wie Selegilin einnehmen, ein erhöhtes Risiko für Selbstmordgedanken und -verhalten besteht.Dies deckt sich mit den Black-Box-Warnungen der FDA für ähnliche MAOI-Medikamente.
-
Herausforderungen bei der Verabreichung
-
Das Standardprotokoll erfordert die tägliche Anwendung auf intakter Haut (Oberarm/Rumpf/Oberschenkel) mit stufenweiser Dosiserhöhung (6mg→12mg über Wochen).Pädiatrische Patienten haben möglicherweise Probleme mit:
- Beständige Pflasterhaftung aufgrund höherer Aktivität
- Präzise Dosierungsanpassung bei geringerer Körpermasse erforderlich
- Risiko der versehentlichen Einnahme, wenn die Pflaster falsch gehandhabt werden
-
Das Standardprotokoll erfordert die tägliche Anwendung auf intakter Haut (Oberarm/Rumpf/Oberschenkel) mit stufenweiser Dosiserhöhung (6mg→12mg über Wochen).Pädiatrische Patienten haben möglicherweise Probleme mit:
-
Alternative Behandlungsmöglichkeiten
Während Selegilin-Pflaster nicht geeignet sind, umfasst die Behandlung pädiatrischer Depressionen in der Regel:- SSRIs mit bewährtem Sicherheitsprofil (z. B. Fluoxetin für ≥8-Jährige)
- Kognitive Verhaltenstherapie als Erstlinientherapie
- Enge Überwachung während der Medikamenteneinführung
-
Regulatorischer Konsens
Mehrere Agenturen für Arzneimittelsicherheit raten einheitlich vom Off-Label-Gebrauch in der Pädiatrie ab und betonen:- Mangel an Wirksamkeitsdaten für Depressionen bei Kindern
- Irreversible MAOI-Effekte, die sich unverhältnismäßig stark auf die sich entwickelnden Neurotransmittersysteme auswirken können
Für die Einkäufer im Gesundheitswesen unterstreicht dies, wie wichtig es ist, altersgerechte Alternativen auf Lager zu haben und sicherzustellen, dass die verschreibenden Ärzte Zugang zu den aktuellen Sicherheitshinweisen für die Verwendung von Antidepressiva in pädiatrischen Bevölkerungsgruppen haben.
Zusammenfassende Tabelle:
| Hauptanliegen | Einzelheiten |
|---|---|
| Altersbeschränkung | Kontraindiziert für Kinder <12 Jahre |
| Suizid-Risiko | Blackbox-Warnung vor Selbstmordgedanken bei jungen Konsumenten |
| Herausforderungen bei der Dosierung | Schwierige Adhäsion & präzise Anpassungen bei geringer Körpermasse |
| Alternativen | SSRIs (z. B. Fluoxetin) + Therapie bevorzugt |
| Regulatorische Haltung | Globale Behörden verbieten Off-Label-Verwendung in der Pädiatrie |
Sie benötigen zuverlässige, altersgerechte transdermale Lösungen? Als zuverlässiger Hersteller von FDA-konformen Pflastern ist Enokon auf sichere Arzneimittelverabreichungssysteme für alle Patientengruppen spezialisiert. Kontaktieren Sie unsere Experten um geprüfte Alternativen für die pädiatrische psychische Behandlung oder maßgeschneiderte F&E für Ihren Bedarf zu besprechen.
Visuelle Anleitung
Ähnliche Produkte
- Silikonpflaster für Narbenblätter Transdermales Medikamentenpflaster
- Menthol Gel Schmerzlinderungspflaster
- Icy Hot Menthol Medizin Schmerzlinderung Patch
- Natürliches pflanzliches Wermutpflaster Schmerzpflaster
- Lidocain-Hydrogel-Pflaster zur Schmerzlinderung
Andere fragen auch
- Wie beeinflusst eine abgedeckte Form oder ein umgedrehter Trichter die Verdunstung von Lösungsmitteln bei transdermalen Pflastern? Optimieren Sie die Filmqualität.
- Welche Rolle spielt ein silikonbasiertes transdermales Verabreichungssystem bei Parkinson? Verbesserung der Versorgung von Patienten im Frühstadium
- Was sind einige häufige Nebenwirkungen bei der Verwendung des transdermalen Pflasters?Risikobeherrschung für eine sichere Anwendung
- Welchen Nutzen hat die Selbstverabreichung von transdermalen Pflastern für die Patienten?Verbesserte Unabhängigkeit und Compliance
- Wie unterstützt die Erfassung von SUSARs die Optimierung von Materialien für transdermale Pflaster? Verbesserung von Sicherheit & Biokompatibilität