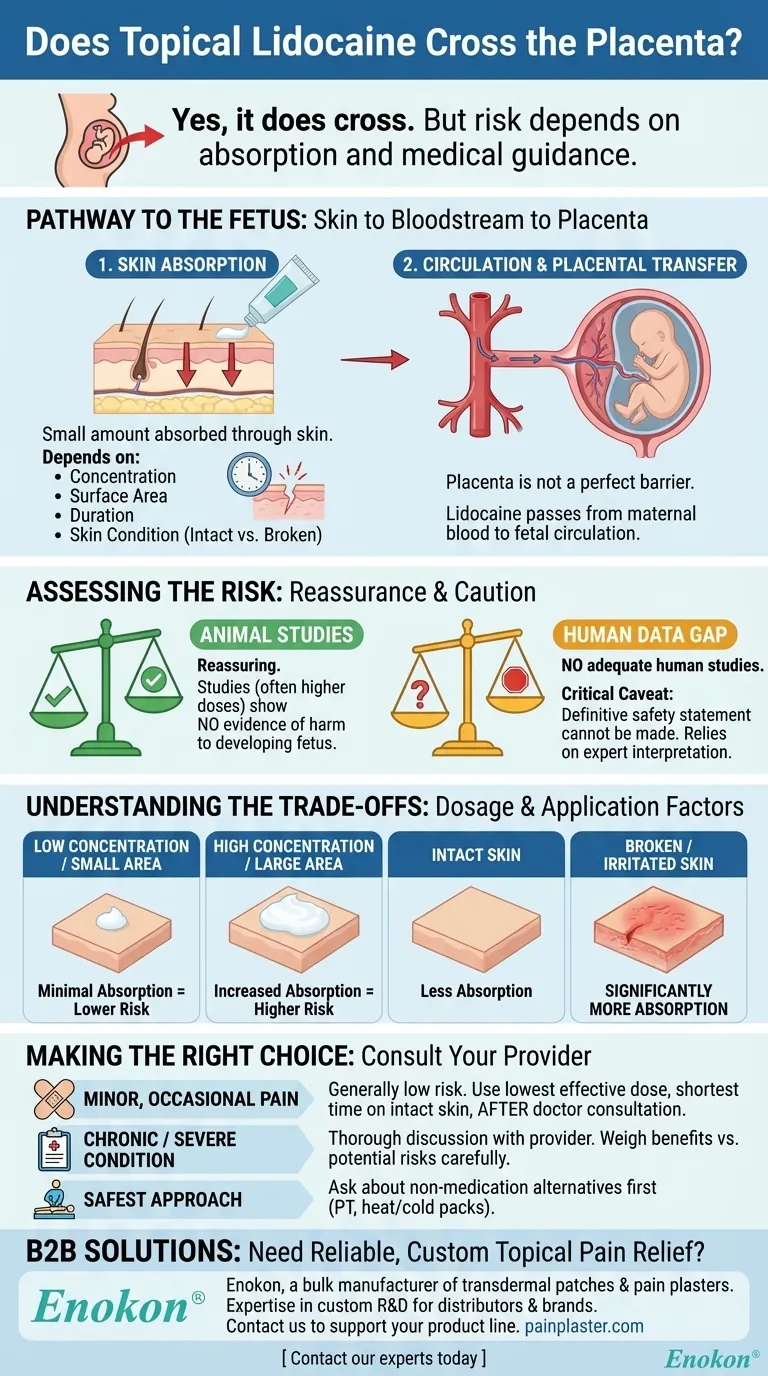
Lidocain topisch passiert die Plazenta, aber die vorliegenden Erkenntnisse aus Tierversuchen deuten nicht auf eine signifikante Schädigung des Fötus hin.Es fehlen jedoch umfassende Humanstudien, um die Sicherheit von Lidocain während der Schwangerschaft vollständig zu bestätigen.Dies führt zu einem vorsichtigen Ansatz bei der klinischen Anwendung, bei dem die potenziellen Vorteile gegen die theoretischen Risiken abgewogen werden.

Die wichtigsten Punkte werden erklärt:
-
Plazenta-Transfer von topischem Lidocain
- Lidocain kann bei topischer Anwendung die Plazentaschranke überwinden.Dies ist auf seine molekularen Eigenschaften zurückzuführen, die es ihm ermöglichen, biologische Membranen, einschließlich der Plazenta, zu durchdringen.
- Das Ausmaß der Übertragung hängt von Faktoren wie der Dosierung, der Applikationsstelle und dem mütterlichen Stoffwechsel ab.
-
Tierstudien und fötale Sicherheit
- Tierversuche haben keine direkte Schädigung von Föten gezeigt, die Lidocain ausgesetzt waren.Diese Studien sind für eine erste Sicherheitsbewertung von entscheidender Bedeutung, können aber nur bedingt zur Vorhersage von Ergebnissen beim Menschen herangezogen werden.
- Die Ergebnisse deuten darauf hin, dass typische therapeutische Dosen in Tiermodellen keine teratogenen Wirkungen oder Entwicklungsanomalien verursachen.
-
Fehlende Humanstudien
- Es gibt keine gut kontrollierten oder groß angelegten Studien an schwangeren Frauen, um die Sicherheit von Lidocain während der Schwangerschaft endgültig zu belegen.
- Diese Datenlücke bedeutet, dass sich Gesundheitsdienstleister bei der Erwägung der Anwendung von Lidocain häufig auf Tierstudien und klinische Beurteilungen verlassen.
-
Klinische Erwägungen
- Bei der Entscheidung über die Anwendung von Lidocain in der Schwangerschaft sollten die Notwendigkeit (z. B. Schmerzlinderung bei kleineren Eingriffen) und die möglichen Risiken abgewogen werden.
- Falls verfügbar, können alternative Behandlungen oder risikoärmere Anästhetika in Betracht gezogen werden.
-
Regulatorische und fachliche Richtlinien
- Die Zulassungsbehörden stufen Lidocain als Arzneimittel der Kategorie B" für die Schwangerschaft ein, was bedeutet, dass bei Tieren kein Risiko nachgewiesen wurde, aber keine ausreichenden Daten für den Menschen vorliegen.
- Fachliche Leitlinien empfehlen häufig eine minimale Anwendung und eine engmaschige Überwachung, wenn Lidocain als notwendig erachtet wird.
Obwohl Lidocain in der Regel als risikoarm gilt, sollte seine Anwendung in der Schwangerschaft von Fall zu Fall sorgfältig geprüft werden.Haben Sie spezifische Szenarien diskutiert, in denen Lidocain für das Wohlbefinden oder die Sicherheit der Mutter unerlässlich sein könnte?
Zusammenfassende Tabelle:
| Wichtige Überlegungen | Einzelheiten |
|---|---|
| Plazentare Übertragung | Lidocain passiert aufgrund seiner molekularen Eigenschaften die Plazenta. |
| Ergebnisse aus Tierstudien | Bei therapeutischen Dosen wurden keine signifikanten Schäden bei Tierföten beobachtet. |
| Datenlücke beim Menschen | Begrenzte Studien an schwangeren Frauen; Vertrauen auf Tierdaten und klinisches Urteil. |
| Kategorie für Schwangere (FDA) | Kategorie B: Kein nachgewiesenes Risiko bei Tieren, aber keine ausreichenden Studien am Menschen. |
| Klinische Empfehlung | Vorsichtig anwenden, Nutzen und Risiken abwägen; wenn möglich, Alternativen in Betracht ziehen. |
Brauchen Sie sichere Lösungen zur Schmerzlinderung während der Schwangerschaft?
Unter
Enokon
sind wir spezialisiert auf
FDA-konforme transdermale Pflaster und Schmerzpflaster
und bietet
kundenspezifische F&E-Unterstützung
für Vertriebsunternehmen und Marken im Gesundheitswesen.Unsere Formulierungen konzentrieren sich auf
Sicherheit und Wirksamkeit
selbst für sensible Bevölkerungsgruppen wie schwangere Patientinnen.
Kontaktieren Sie noch heute unsere Experten um zu besprechen risikoarme topische Analgetika-Optionen die auf Ihre Bedürfnisse zugeschnitten sind.
Visuelle Anleitung
Ähnliche Produkte
- Lidocain-Hydrogel-Pflaster zur Schmerzlinderung
- Ferninfrarot-Wärmepflaster zur Schmerzlinderung Transdermale Pflaster
- Silikonpflaster für Narbenblätter Transdermales Medikamentenpflaster
- Icy Hot Menthol Medizin Schmerzlinderung Patch
- Menthol Gel Schmerzlinderungspflaster
Andere fragen auch
- Wie sollten Lidocain-Pflaster angewendet werden, um eine optimale Wirkung zu erzielen?Maximale Schmerzlinderung bei richtiger Anwendung
- Was sind die häufigsten Nebenwirkungen von Lidocain-Pflastern?Risikobewältigung für sichere Schmerzlinderung
- Wie lauten die Dosierungsrichtlinien für Lidocain-Pflaster?Sichere und wirksame Tipps zur Schmerzlinderung
- Wie lange werden Lidocainpflaster normalerweise verschrieben?Kurzfristige und chronische Schmerzlinderung erklärt
- Welche Vorsichtsmaßnahmen sind bei der Entsorgung von Lidocain-Pflastern zu beachten?Tipps zur sicheren Entsorgung zur Vermeidung von Risiken










