Die Einschlusskriterien für Patienten in der Lidocain-Pflaster 5 Prozent Studie wurden Personen mit bestimmten Schmerzzuständen und stabilen Schmerzmitteln ausgewählt.Bei den Teilnehmern handelte es sich um Erwachsene ab 18 Jahren mit Osteoarthritis in einem oder beiden Knien, die einen konsistenten Schmerzbehandlungsplan einhielten und eine durchschnittliche tägliche Schmerzintensität von über 4/10 auf dem Brief Pain Inventory (BPI) angaben.Die Studie konzentrierte sich auf die Bewertung der Auswirkungen des Pflasters auf die Schmerzqualität bei Erkrankungen wie postherpetische Neuralgie (PHN), diabetische Neuropathie (DN) und Kreuzschmerzen (LBP) unter Verwendung der Neuropathic Pain Scale (NPS).Die Studie war eine offene, nicht-randomisierte und prospektive Studie, die über einen Zeitraum von zwei Wochen an mehreren Standorten in den USA durchgeführt wurde, wobei die Patienten täglich bis zu vier Pflaster auf die Bereiche mit maximalen Schmerzen aufklebten.
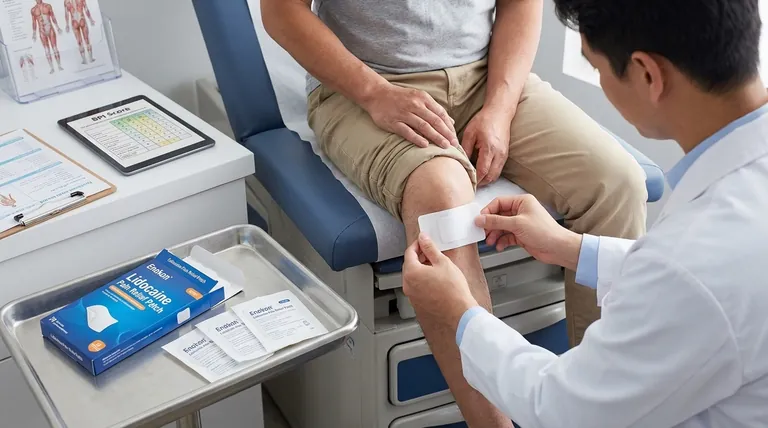
Die wichtigsten Punkte erklärt:
-
Kriterien für Alter und Geschlecht:
- Die Patienten mussten sein 18 Jahre oder älter sein und umfasst sowohl Männer als auch Frauen.Dadurch wird sichergestellt, dass die Studienergebnisse auf die erwachsene Bevölkerung anwendbar sind, die das Pflaster am ehesten klinisch verwendet.
-
Anforderungen an die Diagnose:
- Die Teilnehmer benötigten eine bestätigte Diagnose von Osteoarthritis in einem oder beiden Knien .Diese Spezifität trägt dazu bei, den Schwerpunkt der Studie auf gelenkbezogene chronische Schmerzen zu legen.
- Sekundäre Erkrankungen wie PHN, DN, oder LBP wurden ebenfalls ausgewertet, um den Anwendungsbereich auf neuropathische und muskuloskelettale Schmerzen auszudehnen.
-
Schwellenwert der Schmerzintensität:
- A BPI-Wert >4/10 für den durchschnittlichen täglichen Schmerz war obligatorisch.Mit diesem Grenzwert werden Patienten mit mäßigen bis starken Schmerzen identifiziert, um sicherzustellen, dass die Wirksamkeit des Pflasters in klinisch relevanten Szenarien getestet wird.
-
Stabiles Analgetikaregime:
- Die Patienten wurden aufgefordert, ihre bestehende Schmerztherapiepläne ohne Dosisanpassung beibehalten .Auf diese Weise werden Störvariablen ausgeschlossen und die additive Wirkung des Pflasters isoliert.
-
Anwendung Protokoll:
- Die Pflaster wurden aufgeklebt auf intakte Haut (keine Blasen) an der Stelle des maximalen Schmerzes mit einer Obergrenze von vier Pflastern pro 24 Stunden .Auf diese Weise wird die Behandlung standardisiert und gleichzeitig die reale Anwendung nachgeahmt.
-
Studienaufbau:
- Die offene, nicht-randomisierte, prospektive Design über sieben U.S.-Standorten bietet pragmatische Einblicke, auch wenn sie nicht die Strenge von Blindstudien aufweist.Die Website 2-wöchige Dauer schafft ein Gleichgewicht zwischen Praktikabilität und ausreichender Zeit zur Beobachtung der Wirkungen.
-
Sicherheit und Verträglichkeit:
- Sowohl das aktive als auch das Vehikelpflaster zeigten niedrige Raten unerwünschter Ereignisse die das Sicherheitsprofil des Pflasters untermauern - eine wichtige Überlegung für Kostenträger, die das Risiko-Nutzen-Verhältnis bewerten.
Durch die Einhaltung dieser Kriterien wurde in der Studie eine homogene Patientenpopulation sichergestellt, was die Zuverlässigkeit der Ergebnisse für Gesundheitsdienstleister und Käufer, die die Eignung des Pflasters für die Behandlung chronischer Schmerzen beurteilen, erhöht.Würde die Einbeziehung einer breiter angelegten Schmerzskala wie des NPS dazu beitragen, die Verwendung des Pflasters in künftigen Untersuchungen auf bestimmte Schmerzsubtypen zuzuschneiden?
Zusammenfassende Tabelle:
| Kriterien | Anforderung |
|---|---|
| Alter | 18 Jahre oder älter |
| Diagnose | Arthrose in einem/beiden Knien; sekundäre Erkrankungen (PHN, DN, LBP) untersucht |
| Schmerzintensität (BPI) | >4/10 durchschnittliche tägliche Schmerzen |
| Analgetika-Schema | Stabil, keine Dosisanpassung |
| Anwendung des Pflasters | Bis zu 4 Pflaster/24 Stunden auf intakter Haut an der Stelle mit den größten Schmerzen |
| Studienaufbau | Offene, nicht-randomisierte, prospektive Studie (2 Wochen, 7 US-amerikanische Standorte) |
| Sicherheitsprofil | Niedrige Raten unerwünschter Ereignisse bei aktiven Pflastern/Vehikelpflastern |
Sie benötigen klinisch validierte Lösungen zur Schmerzlinderung? Partnerschaft mit Enokon ist ein zuverlässiger Hersteller von transdermalen Pflastern und Schmerzpflastern für Gesundheitsdienstleister und Pharmamarken.Unser Know-how in der kundenspezifischen Forschung und Entwicklung gewährleistet maßgeschneiderte Formulierungen für die Behandlung chronischer Schmerzen. Kontaktieren Sie uns um zu besprechen, wie unsere Lidocain-Pflaster die Bedürfnisse Ihrer Patienten mit nachgewiesener Sicherheit und Wirksamkeit erfüllen können.
Visuelle Anleitung
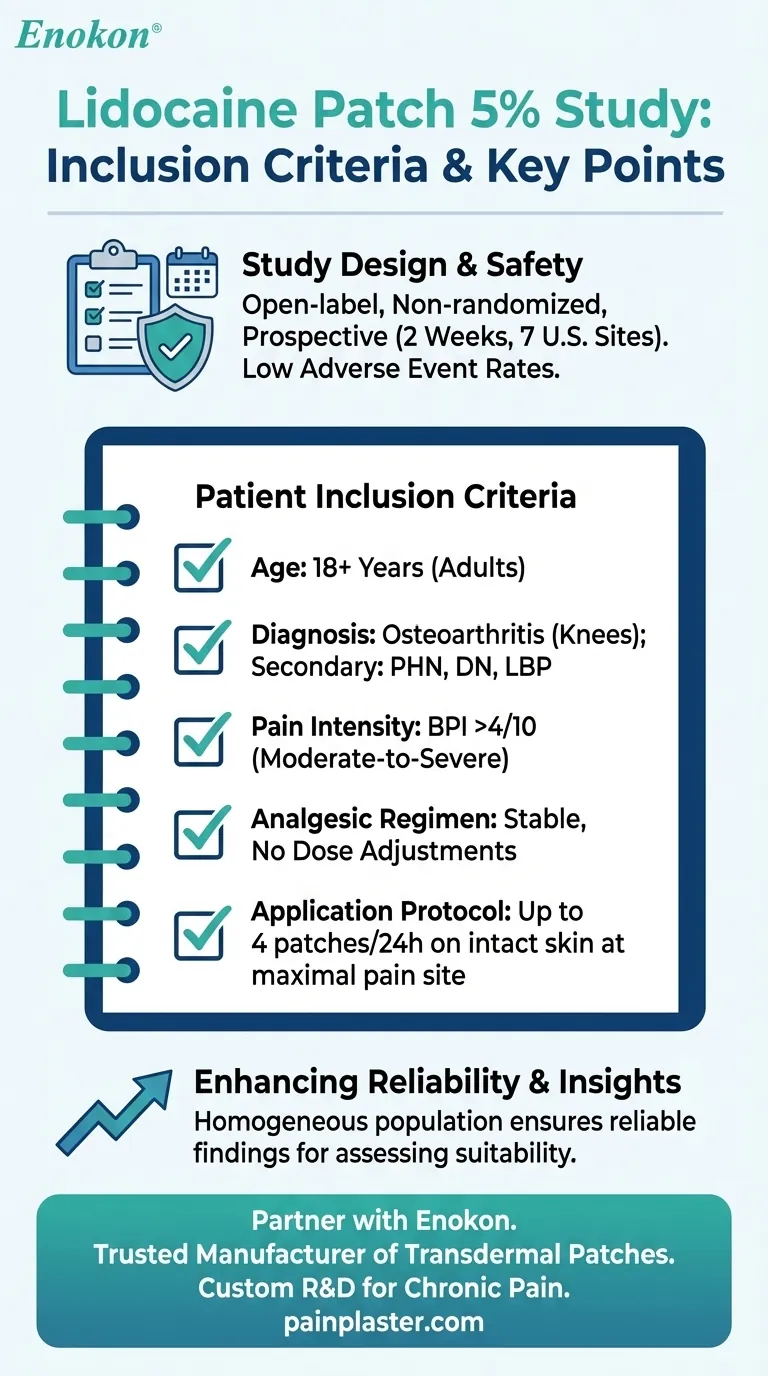
Ähnliche Produkte
Andere fragen auch
- Wird ein Hausarzt routinemäßig Lidocain-Pflaster auch nach der Anfangsphase verschreiben?Leitlinien zur Langzeitanwendung verstehen
- Was sind Lidocain-Pflaster und wie funktionieren sie?Gezielte Schmerzlinderung erklärt
- Was sind die häufigsten Nebenwirkungen von Lidocain-Pflastern?Risikobewältigung für sichere Schmerzlinderung
- Wie unterscheiden sich Lidocain-Pflaster in ihrem Wirkmechanismus von Icy Hot und Biofreeze-Pflastern?
- Welche Vorsichtsmaßnahmen sind bei der Entsorgung von Lidocain-Pflastern zu beachten?Tipps zur sicheren Entsorgung zur Vermeidung von Risiken
